控制无菌洁净室手套上的内毒素污染

被内毒素污染的注射药品或植入式医疗器械可能会引起非常严重的患者反应。
批量注射溶液或植入物的内毒素污染也会给制造商带来重大的财务后果。
因此,监测无菌洁净室丁腈手套和乳胶手套的内毒素污染是关键环境(包括植入式医疗器械行业和制药行业)的一个关键问题。
什么是细菌内毒素及其影响?
什么是细菌内毒素?
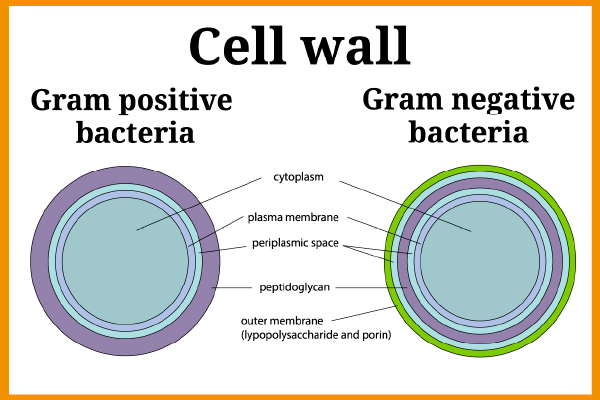
内毒素或脂多糖 (LPS) 是革兰氏阴性细菌外膜的碎片(使用革兰氏染色技术,革兰氏阴性细菌产生粉红色染色,而革兰氏阳性细菌则产生紫色)。 革兰氏阴性菌的一些例子有大肠杆菌、沙门氏菌、军团菌、奈瑟氏菌等。
图 1 – 革兰氏阳性和革兰氏阴性细菌的细胞壁
革兰氏阴性细菌存在于环境中的任何地方(水、加热系统、消化道和粪便……),因此内毒素的存在可能会带来非常高的风险。 内毒素分子在裂解过程中释放(在物理、化学或生物制剂的作用下破坏细胞膜)。
内毒素污染会造成什么后果?
内毒素的生物组成会影响人类和动物的免疫系统,并可能引起过敏反应。 因此,它们会导致相对强烈的炎症反应。 它们还可能导致体弱(免疫功能低下)、年轻(早产儿)或老年患者的严重感染。
最常见的反应是发烧。 这就是为什么革兰氏阴性内毒素被认为是“热原” ,即通过激活免疫系统引发体温升高的分子。
吸入内毒素也可能导致急性呼吸窘迫综合征 (ARDS)。 注射后进入体内,内毒素可引起弥散性血管内凝血,当大量进入血液时甚至引起感染性休克。
在制药行业等关键环境中,内毒素监测至关重要。 在医药级水(纯化水)的生产以及肠胃外和注射药物的制造(输液液、透析液……)和植入式医疗设备中尤其如此。
降低洁净室手套的内毒素水平
已知内毒素是药品和医疗器械中最常见的热原来源。
内毒素是革兰氏阴性菌的膜残留物。 后者在环境中是可行的且数量众多。 此外,内毒素对包括伽马射线照射在内的消毒或灭菌过程具有高度抵抗力。
这就是为什么在灭菌前应尽可能限制丁腈和乳胶手套的生物负载。
生物负荷是表面或设备中各种活微生物的浓度。 该生物负载主要来自:
- 生产过程中使用的原材料(包括医药级水)。
- 参与制造过程的操作员。
- 制成品的清洁和包装操作。
SHIELD Scientific无菌手套上微生物污染的检测和定量由外部组织根据 ISO 11737-1 进行。 它是SHIELD Scientific质量控制流程的基本组成部分。
因此,用于制造药品或植入式医疗器械的所有原材料、包装或防护设备必须符合无菌和热原性的健康要求。
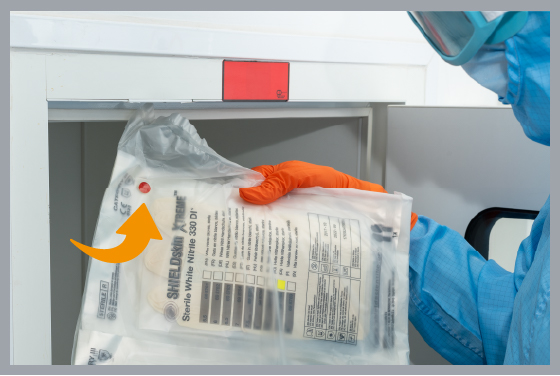
无菌:为了确保无菌保证水平 (SAL) 为 10-6(根据欧洲药典的要求),手套必须根据 ISO 11137-2:2015(保健品灭菌 – 辐射 – 部分)进行微生物验证2:确定灭菌剂量)。
图 2 – 带灭菌指示器的SHIELDskin XTREME™无菌手套 PE 袋
无热原性:去热原可以通过多种方式完成:
- 用注射用水 (WFI) 或其他高级水(例如去离子水)清洗。
- 通过暴露在高温下进行干热处理。
- 通过压力和过氧化氢的组合进行湿热处理(警告:高压灭菌器不会破坏内毒素)。
- 根据内毒素的分子量对其进行超滤。
- 被环氧乙烷破坏。
为什么控制无菌洁净室手套的内毒素水平很重要?
对于许多药品和植入式医疗器械制造商来说,无菌要求(不存在活微生物)和热原性(不存在内毒素等热原分子)至关重要。
为了尽可能限制与内毒素相关的风险,从原材料到成品的整个生产过程中控制污染
事实上,戴手套的手可以直接接触注射溶液或其容器和可植入医疗设备。 因此,手套是潜在的污染源。
图 3 – 佩戴双副SHIELD Scientific无菌手套的操作员更换灌装机针头
标准丁腈和乳胶一次性手套在完成浸渍和干燥步骤后只需要进行最少的处理。 因此,手套的清洁度水平可能不适合洁净室应用。 另外值得注意的是,手套可能含有大量革兰氏阴性细菌。 即使是通常经过氯化并用纯净水清洗的无菌洁净室手套,通常也无法保证内毒素水平。
此外,由于颗粒可以传播内毒素,因此选择颗粒含量“保证低水平”的手套可能有助于加强您的污染控制策略。
因此,选择内毒素含量低(EN 455-3:2015 中定义的<20 EU/副)的手套,甚至更好的是经过批量内毒素测试的手套可能是一种解决方案。
无菌洁净室手套的内毒素水平如何监测?
无菌手套内毒素污染相关监管框架
欧盟 GMP 附件 1是管理药品生产和控制的主要文件之一。 本文件提供质量风险管理指南。 特别是,新 GMP 的附录 I 规定必须避免最终产品的微生物、颗粒物和内毒素/热原污染。 因此,无菌洁净室手套必须纳入质量风险管理 (QRM)。
EN 455-3:2015 (一次性医用手套 - 第 3 部分:生物学评估的要求和测试)要求无菌一次性手套的制造商控制手套的内毒素污染。 试验方法应符合欧洲药典专论2.6.14的要求。
鲎检测内毒素
用于测量无菌洁净室手套上细菌内毒素水平的最广泛使用和认可的方法是使用 鲎变形细胞裂解物 (LAL) 的方法。
鲎是一种古老的海洋节肢动物,具有蓝色血液(或者更确切地说,对于无脊椎动物来说是血淋巴)的特性。
图 4 – 鲎-Limulus polyphemus
这种血淋巴含有卵圆形的变形细胞,在内毒素存在时,变形细胞会失去这种形状并聚集成凝块。 鲎血液的凝固是各种内毒素测定测试方法的基础。
无菌手套内毒素污染测定的试验方法
首先将一副手套的外表面用40至50毫升无内毒素水(符合欧洲药典的LAL水)在37°C至40°C的温度下提取40至60分钟如有必要,然后将提取物离心(2,000 g,15 分钟)以除去颗粒。 然后将其倒出,然后立即进行内毒素测试。
使用鲎变形细胞裂解物检测细菌内毒素的方法主要有3种:
- 凝胶凝块测试(“定性”测试=可以检测内毒素的存在,但无法精确确定数量):提取物和鲎试剂混合后形成凝胶(“凝块”)。
- 动力学比浊法测试(“定量”测试=允许检测内毒素的存在并确定数量):与鲎试剂混合后出现浊度。
- 显色测试(“定量”测试=允许检测内毒素的存在并确定数量):与鲎试剂混合后显色。
检测结果以每副手套的内毒素单位 (EU) 报告。
EN 455-3:2015 规定,为了贴上“低内毒素含量”标签,手套的内毒素含量限值必须为每双手套 20 EU。
适用于关键环境的SHIELD Scientific低内毒素含量无菌手套
为了限制患者出现某些并发症的风险,应注意使用内毒素含量低的优质无菌手套。
作为整体污染控制和质量风险管理 (QRM) 策略的一部分,考虑手套的选择以及如何将其应用于您的关键环境可能会有所帮助。
这就是为什么SHIELD Scientific开发了一系列丁腈和乳胶洁净室手套,这些手套提供与去离子水洗涤量直接相关的不同清洁度级别。 对于该系列的一次性手套,有一个简单的分类:
DI:手套在去离子水中单次清洗,用于基本污染控制和颗粒水平规格 < 3,000 个/cm² > 0.5μm。
DI+ :手套在去离子水中清洗三次,以实现高污染控制和颗粒水平规格 < 1,200 个/cm² > 0.5μm。
DI++ :手套经过去离子水多次清洗,以实现极端的污染控制,颗粒水平规格 < 850 个/cm² > 0.5μm。
所有SHIELDskin XTREME™品牌无菌手套的设计均符合 GMP 操作人员要求的质量标准,以降低污染风险。 所有SHIELD Scientific洁净室丁腈和乳胶无菌手套均经过批量测试,证明每副手套的内毒素含量 < 20 UE(内毒素单位),无菌保证水平 (SAL) 为 10-6(通过伽马辐照灭菌)。
每批SHIELD Scientific无菌丁腈和乳胶洁净室手套均附有辐照证书 (CoI)。 合格证书 (CoC) 提供有关颗粒和内毒素水平的批次特定数据。
由于控制内毒素污染在关键环境中至关重要,因此请立即订购样品或向SHIELD Scientific销售代表。
分享这个有趣的信息