無菌クリーンルーム用手袋のエンドトキシン汚染の制御

エンドトキシンで汚染された注射用医薬品または埋め込み型医療機器は、患者に非常に重篤な反応を引き起こす可能性があります。
注射用溶液またはインプラントのバッチのエンドトキシン汚染も、メーカーに重大な経済的影響を与える可能性があります。
したがって、無菌クリーンルームのニトリル手袋やラテックス手袋のエンドトキシン汚染の監視は、埋め込み型医療機器産業や製薬産業などの重要な環境にとって重要な懸念事項です。
細菌のエンドトキシンとその影響とは何ですか?
細菌エンドトキシンとは何ですか?
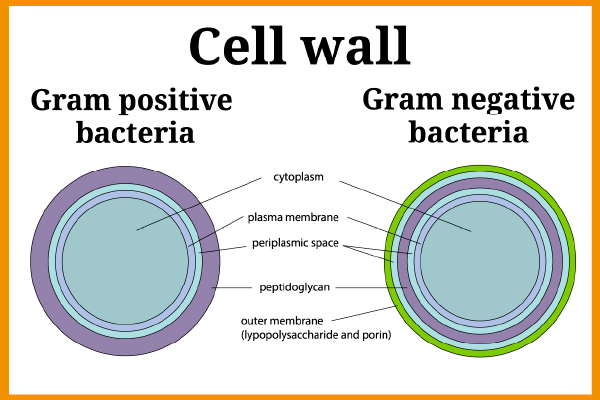
エンドトキシンまたはリポ多糖類 (LPS) は、グラム陰性菌の外膜の断片です (グラム染色技術を使用すると、グラム陰性菌はピンク色の染色を生成しますが、グラム陽性菌の場合は紫色になります)。 グラム陰性菌の例としては、大腸菌、サルモネラ菌、レジオネラ菌、ナイセリア菌などが挙げられます。
図 1 – グラム陽性菌とグラム陰性菌の細胞壁
グラム陰性菌は環境中のあらゆる場所(水、暖房システム、消化管、糞便など) にため、エンドトキシンの存在は非常に高いリスクを引き起こす可能性があります。 エンドトキシン分子は、溶解(物理的、化学的、または生物学的因子の作用による細胞膜の破壊)中に放出されます。
エンドトキシン汚染の影響は何ですか?
エンドトキシンの生物学的構成は人間や動物の免疫系に影響を与え、アレルギー反応を引き起こす可能性があります。 その結果、比較的強い炎症反応を引き起こす可能性があります。 また、衰弱した患者(免疫力が低下した患者)、若い患者(早産児)、または高齢の患者において重篤な感染症を引き起こす可能性があります。
最も一般的な反応は発熱です。 これが、 、つまり免疫系を活性化することによって体温上昇を引き起こす分子であると考えられる
エンドトキシンを吸入すると、急性呼吸窮迫症候群 (ARDS) を引き起こす可能性もあります。 注射後に体内に入ると、エンドトキシンは播種性血管内凝固症候群を引き起こしたり、大量に血流に到達すると敗血症性ショックを引き起こす可能性があります。
製薬業界のような重要な環境では、エンドトキシンのモニタリングが不可欠です。 これは、医薬品グレードの水 (精製水) の製造に加え、非経口薬および注射薬 (輸液、透析液など) および埋め込み型医療機器の製造に特に当てはまります。
クリーンルーム用手袋のエンドトキシンレベルの低減
エンドトキシンは、医薬品や医療機器における発熱物質の最も一般的な発生源であることが知られています。
エンドトキシンはグラム陰性菌の膜残留物です。 後者は環境中に生存可能であり、多数存在します。 さらに、エンドトキシンは、ガンマ線照射を含む消毒または滅菌プロセスに対して非常に耐性があります。
このため、滅菌前にニトリル手袋とラテックス手袋の微生物負荷を可能な限り制限する必要があります。
バイオバーデンとは、表面またはデバイス内のあらゆる種類の生存可能な微生物の濃度です。 このバイオバーデンは主に次のものから発生します。
- 製造工程で使用される原材料(医薬品グレードの水を含む)。
- 製造工程に携わるオペレーター。
- 製造された製品の洗浄と梱包作業。
SHIELD Scientific滅菌手袋の微生物汚染の検出と定量化は、ISO 11737-1 に従って外部組織によって行われます。 これはSHIELD Scientificの品質管理プロセスの基本的な部分です。
したがって、医薬品または埋め込み型医療機器の製造に使用されるすべての原材料、包装、保護具は、無菌性だけでなく発熱性についても健康要件を満たさなければなりません。
無菌性: 10-6 (欧州薬局方の要件に従って) の無菌保証レベル (SAL) を確保するには、手袋は ISO 11137-2:2015 (ヘルスケア製品の滅菌 – 放射線 – パート) に従って微生物学的検証を受ける必要があります。 2: 滅菌量の設定)。
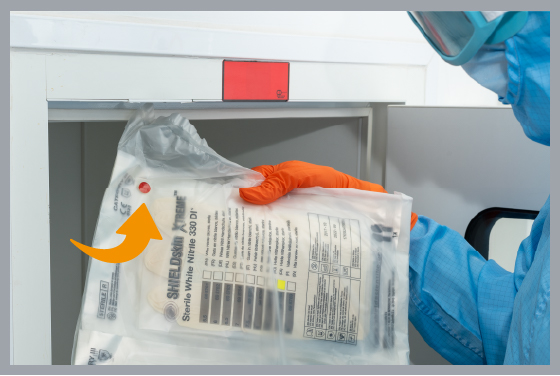
図 2 – SHIELDskin XTREME™滅菌手袋 滅菌インジケーター付き PE バッグ
非発熱性:脱発熱性はさまざまな方法で行うことができます。
- 注射用水 (WFI) または脱イオン水などのその他の高級水による洗浄。
- 高温にさらす乾熱処理。
- 圧力と過酸化水素の組み合わせによる湿熱処理 (警告: オートクレーブはエンドトキシンを破壊しません)。
- 分子量に応じたエンドトキシンの限外濾過。
- エチレンオキシドによる破壊。
無菌クリーンルーム用手袋のエンドトキシンレベルを管理することがなぜ重要なのでしょうか?
無菌性要件 (生きた微生物が存在しないこと) と発熱性 (エンドトキシンなどの発熱性分子が存在しないこと) は、医薬品および埋め込み型医療機器の多くのメーカーにとって最重要事項です。
したがって、エンドトキシンに関連するリスクを可能な限り制限するには、クリーンルーム作業員の保護具を含め、原材料から最終製品に至る生産プロセス全体にわたって汚染を管理する必要があります
実際、手袋をした手は、注射液やその容器、埋め込み型医療機器に直接接触する可能性があります。 したがって、手袋は潜在的に汚染源となります。
図 3 – SHIELD Scientific滅菌手袋を 2 枚着用したオペレーターによって交換された充填機の針
標準的なニトリルおよびラテックスの使い捨て手袋は、浸漬および乾燥のステップが完了すると最小限の処理を受けます。 したがって、手袋の清浄度レベルはクリーンルーム用途には許容できない可能性があります。 また、手袋にはグラム陰性菌が大量に付着している可能性があることにも注意してください。 通常は塩素処理され、精製水で洗浄される無菌のクリーンルーム用手袋でさえ、エンドトキシンレベルの点で保証がないことがよくあります。
さらに、粒子はエンドトキシンを媒介する可能性があるため、「低レベルが保証された」粒子を含む手袋を選択することは、汚染管理戦略の強化に役立つ可能性があります。
したがって、エンドトキシンの含有量が低い手袋 (EN 455-3:2015 で定義されているように、1 組あたり 20 EU 未満)、さらにはエンドトキシンのバッチテストが行われている手袋を選択することが解決策となる可能性があります。
無菌クリーンルーム用手袋のエンドトキシンレベルはどのように監視されますか?
滅菌手袋のエンドトキシン汚染に関する規制枠組み
欧州連合の GMP の附属書 1 は、医薬品の製造と管理を管理する主要文書の 1 つです。 この文書は、品質リスク管理のガイドラインを提供します。 特に、新しい GMP の附属書 I では、最終製品の微生物、粒子、エンドトキシン/発熱物質による汚染を回避する必要があると規定しています。 したがって、滅菌クリーンルーム手袋は品質リスク管理 (QRM) に統合する必要があります。
EN 455-3:2015 (使い捨て医療用手袋 – パート 3: 生物学的評価のための要件とテスト) では、滅菌使い捨て手袋のメーカーに対し、手袋のエンドトキシン汚染を管理することが求められています。 試験方法は、欧州薬局方モノグラフ 2.6.14 の要件に準拠するものとします。
エンドトキシンを検出するカブトガニ
滅菌クリーンルーム用手袋の細菌エンドトキシンのレベルを測定するために最も広く使用され、認識されている方法は、 リムルス アメーボサイト ライセート (LAL) を使用する方法です。
カブトガニは、青い血(無脊椎動物の場合は血リンパ)を持つという特徴を持つ祖先海洋節足動物です。
図 4 – カブトガニとカブトガニのカブトガニ
この血リンパには卵形の形状をした変形球細胞が含まれており、エンドトキシンの存在下でこの形状を失い、凝集して血塊になります。 このカブトガニの血液の凝固は、さまざまなエンドトキシン測定法の基礎となります。
滅菌手袋のエンドトキシン汚染を判定するための試験方法
まず、手袋の外面を、37 °C ~ 40 °C の温度で 40 ~ 60 分間、40 ~ 50 ml のエンドトキシンを含まない水 (欧州薬局方に準拠した LAL 水) で抽出します。次に、必要に応じて、抽出物を遠心分離(2,000 g、15 分間)して粒子を除去します。 その後、デカントしてすぐにエンドトキシン検査を行います。
Limulus Amebocyte Lysate を使用した細菌エンドトキシン検査方法は主に 3 つあります。
- ゲル凝固試験(「定性」試験 = エンドトキシンの存在は検出できるが、量を正確に決定することはできない): 抽出物と LAL 剤を混合した後のゲル (「凝固」) の形成。
- 速度論的濁度測定試験(「定量的」試験 = エンドトキシンの存在を検出し、量を決定することができます): LAL 試薬と混合した後の濁度の発生。
- 発色試験(「定量的」試験 = エンドトキシンの存在を検出し、その量を決定することができます): LAL 試薬と混合した後の発色。
試験結果は、手袋 1 組あたりのエンドトキシン単位 (EU) で報告されます。
EN 455-3:2015 では、 「低エンドトキシン含有量」と表示されるためには、手袋のエンドトキシン含有量の制限が 1 組あたり 20 EU でなければならないと規定されています。
SHIELD Scientific重要な環境用の低エンドトキシン含有滅菌手袋
患者における一部の合併症のリスクを制限するには、エンドトキシン含有量が低い高品質の滅菌手袋を使用するように注意する必要があります。
の一環として、手袋の選択と、それが重要な環境にどのように適用されるかを考えると役立つ場合があります。
そのため、 SHIELD Scientific脱イオン水での洗浄量に直接関係するさまざまなレベルの清浄度を提供する、ニトリルおよびラテックスのクリーンルーム用手袋を開発しました。 この範囲の使い捨て手袋には、簡単な分類があります。
DI:基本的な汚染管理および粒子レベル仕様 < 3,000/cm2 > 0.5μm の
ために脱イオン水で単独洗浄された手袋 DI+ 高度な汚染制御と粒子レベル仕様 < 1,200/cm2 > 0.5μm を実現
するために、脱イオン水で 3 回洗浄された手袋 DI++ :極度の汚染制御および粒子レベル仕様 < 850/cm2 > 0.5μm のために脱イオン水で複数回洗浄された手袋。
SHIELDskin XTREME™ブランドの滅菌手袋はすべて、汚染のリスクを軽減するために GMP に準拠して作業するオペレーターが要求する品質基準を満たすように設計されています。 すべてのSHIELD Scientificクリーンルーム用ニトリルおよびラテックス滅菌手袋は、手袋 1 組あたり 20 UE (エンドトキシン単位) 未満の低エンドトキシン含有量と、10-6 (ガンマ線照射滅菌による) の滅菌保証レベル (SAL) を実証するためにバッチテストされています。
SHIELD Scientific滅菌ニトリルおよびラテックスのクリーンルーム用手袋の各バッチには、照射証明書 (CoI) が付属しています。 適合証明書 (CoC) は、粒子とエンドトキシンのレベルに関するバッチ固有のデータを提供します。
サンプルを注文したり、 SHIELD Scientific営業担当者にアドバイスを求めたりするのに今すぐお時間がかかります。
この興味深い情報を共有してください